来源:《农药》2026 ,65 (02)
作者:唐盛东; 杜晓文; 刘东东; 张静; 张立新(1.沈阳化工大学功能分子研究所,辽宁省绿色功能分子设计与开发重点实验室,沈阳市靶向农药重点实验室 2.辽宁科技大学化学工程学院 3.广西思钺生物科技有限责任公司)
螨类是地球上物种多样性最高的节肢动物之一,全球已记录超过5万种,其中农业害螨在分类学上亦呈现显著多样性。这些害螨通过其刺吸式口器取食,破坏植物叶肉组织,导致细胞内容物外泄,进而引发叶片失绿、卷曲、甚至形成锈斑等典型为害症状。在为害严重时,可造成作物系统性损伤,甚至导致整株死亡。目前的害螨综合治理(Integrated Pest Management,IPM)策略包括生物、物理及化学防治等多种手段,其中化学杀螨剂因其高效、速效的特点,在害螨的应急控制和大规模防治中仍占据着核心地位。
然而,由于长期且往往不规范的施用,全球范围内的害螨种群已对多种传统杀螨剂产生了广泛抗性。其抗性机制复杂多样,主要涉及代谢解毒酶(如细胞色素P450单加氧酶、谷胱甘肽-S-转移酶和羧酸酯酶等)的活性增强,以及靶标蛋白的基因突变导致敏感性下降等。因此,开发具有新颖作用模式和高效活性的杀螨剂,以应对日益严峻的抗性挑战,已成为农业化学研究领域的迫切需求。
三氟乙基硫醚(亚砜)类化合物是一类极具开发潜力的新型杀螨活性分子。德国拜耳公司成功开发的sulfiflumin(R-构型亚砜,C14H11F7N2O2S2, CAS登记号2377084-09-6)便是其中的杰出代表,其化学结构如图1所示。该化合物表现出卓越的杀螨活性,为抗性害螨的治理提供了全新的解决方案。
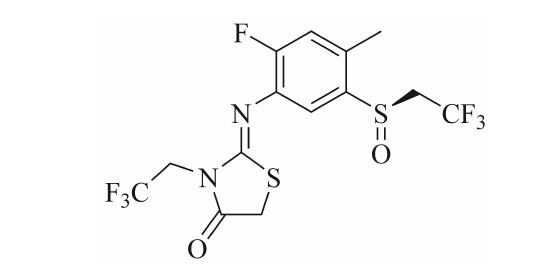
图1 Sulfiflumin的化学结构式
为了探索sulfiflumin在农业害螨防治领域的应用前景以及硫醚与手性亚砜官能团对三氟乙基硫醚(亚砜)类化合物杀螨活性的影响,本实验以2-氟-4-甲基苯胺为起始原料,通过6步反应合成得到了目标硫醚中间体SD-01,并进一步通过不对称催化氧化反应制备了R-构型亚砜类化合物sulfiflumin(见图2)。之后在温室条件下,初步评价了SD-01和sulfiflumin对朱砂叶螨(Tetranychus cinnabarinus)的生物活性。
本研究还开展了初步的分子模拟实验。尽管sulfiflumin的精确靶标尚待最终确证,但乙酰胆碱酯酶(Acetylcholinesterase, AChE)是多种杀虫剂(包括部分杀螨剂)的关键靶点,且已有研究采用分子对接技术模拟了有机磷类、植物提取物等多种分子与AChE的相互作用模式。鉴于此,实验将sulfiflumin与人源重组AChE进行了分子对接,旨在初步探索其与该靶标蛋白的潜在结合模式。同时,利用Gaussian量子化学计算软件,对sulfiflumin和SD-01的分子构象进行了几何优化和前线轨道能级计算,旨在从分子能量学的角度,探讨氧化前后硫醚和亚砜电子结构的变化与其杀螨活性差异的内在联系。文章将为该类杀螨剂的进一步结构优化和作用机制阐明提供参考依据。
材料和方法
1. 实验材料
2-氟-4-甲基苯胺、乙酰氯、甲醛次硫酸钠二水合物,化学纯,宝鸡市国康生物科技有限公司;氯磺酸、盐酸,化学纯,无锡迈默拓普生物科技有限公司;冰乙酸、三乙胺、石油醚、N,N-二甲基甲酰胺,分析纯,天津市恒兴化学试剂制造有限公司;红磷、碘、氯化亚砜、甲苯、碳酸钾、无水硫酸镁、溴乙酸甲酯、二氯甲烷,分析纯,国药集团化学试剂有限公司;2,2,2-三氟碘乙烷、乙酰丙酮铁、苯甲酸钠、1,1,1-三氟-2-异硫氰基乙烷,化学纯,上海麦克林生化科技股份有限公司;2,4-二氯-6-((E)-(((2R)-1-羟基-3,3-二甲基丁-2-基)亚氨基)甲基)苯酚,化学纯,深圳爱拓化学有限公司。
2. 分析测试仪器
AVANCEⅢ600 MHz核磁共振波谱仪,瑞士Bruker公司;Accurate-Mass Q-TOF ESI-MS型质谱仪,美国Agilent公司;CHEETAH中压快速纯化制备色谱,天津博纳艾杰尔科技有限公司。
3. 化合物的合成
以2-氟-4-甲基苯胺为原料,经酰化、还原、水解、醚化反应制得中间体SD-01,后经手性催化氧化制得sulfiflumin,反应条件温和、原料易得,以下为详细合成过程(见图2)。
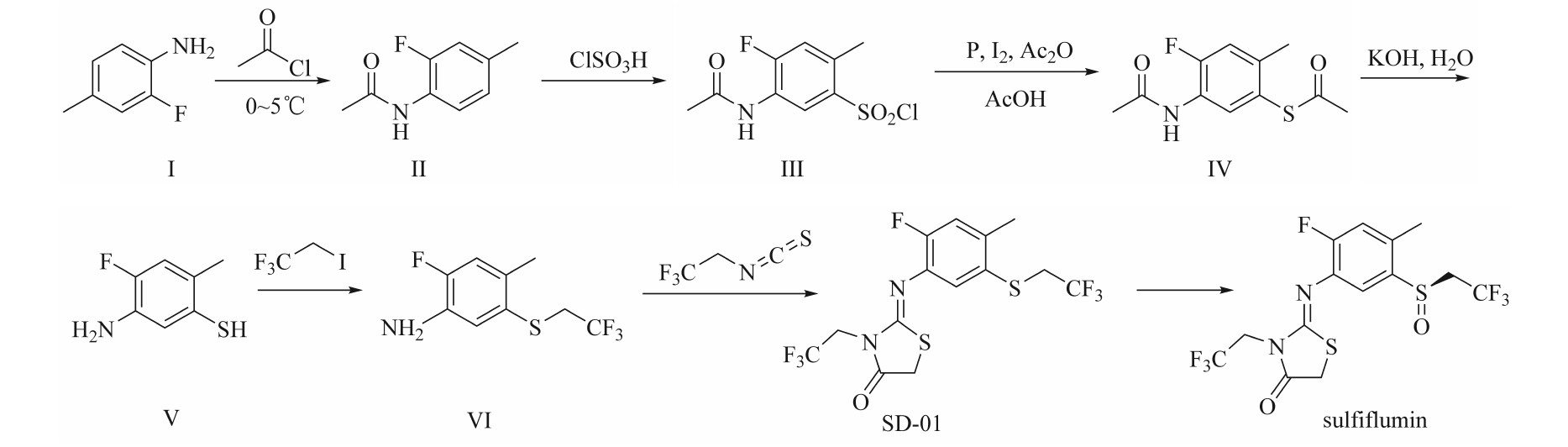
图2 中间体SD-01和sulfiflumin的合成路线
3.1 中间体2-氟-4-甲基乙酰苯胺(Ⅱ)的合成
向100 mL三口瓶中加入2-氟-4-甲基苯胺5.00 g(39.80 mmol)、三乙胺5.99 g(59.19 mmol)和二氯甲烷35 mL,降温至0℃,缓慢滴加乙酰氯3.65 g(46.49 mmol)与二氯甲烷(15 mL)的混合溶液,过程控温0~5℃,30min内滴加完毕。反应体系搅拌升温至20~25℃并保温2 h。TLC监测反应结束,过滤,滤饼用20 mL二氯甲烷洗涤3次。所得固体依次用2 mol/L稀盐酸和100 mL石油醚洗涤,抽滤,滤饼干燥,得到白色固体2-氟-4-甲基乙酰苯胺(Ⅱ)6.20 g,收率95.4%,熔点95.5~97.1℃。1H NMR(600 MHz,CDCl3)δ:9.03(s,1H),7.57(dd,J=7.6,5.0 Hz,1H),7.01(ddd,J=7.4,2.6,0.9 Hz,1H),6.99~6.97(m,1H),2.35(d,J=0.7 Hz,3H),2.17(s,3H)。ESI-MS(m/z):[M+H]+测试值168.07。
3.2 中间体6-甲基-3-乙酰氨基-4-氟苯基磺酰氯(Ⅲ)的合成
向250 mL三口瓶中加入2-氟-4-甲基乙酰苯胺(Ⅱ)6.20 g(37.11 mmol),降温至0℃。向反应体系中滴加氯磺酸22.5 mL(343.5 mmol),过程控温0~10℃,1.5 h滴加完毕。反应体系搅拌升温至70℃并保温5 h。TLC监测反应结束,反应液降至室温后缓慢滴加至150 mL冰水中,过滤,滤饼用饱和食盐水洗涤3次,并用100 mL石油醚洗涤,抽滤,滤饼干燥得白色固体6-甲基-3-乙酰氨基-4-氟苯基磺酰氯(Ⅲ)7.66 g,收率77.8%,熔点94.6~96.2℃。1H NMR(600 MHz,CDCl3)δ:9.18(s,1H),7.82(d,J=4.9 Hz,1H),7.22(d,J=8.1 Hz,1H),2.70(s,3H),2.17(s,3H)。ESI-MS(m/z):[M+H]+测试值266.00。
3.3 中间体4-甲基-5-乙酰硫基-2-氟-N-乙酰苯胺(Ⅳ)的合成
向100 mL三口瓶中加入6-甲基-3-乙酰氨基-4-氟苯基磺酰氯(Ⅲ)7.32 g(27.62 mmol)、50 mL冰乙酸,室温搅拌均匀后加入红磷1.45 g(46.81 mmol)与碘0.15 g(0.59 mmol)。反应体系搅拌升温至110℃并保温3 h。TLC监测反应结束,反应液降温过滤,滤液减压旋蒸,浓缩液缓慢滴加至200 mL冰水中,过滤,滤液萃取,有机相用无水硫酸镁干燥,减压旋蒸,浓缩液冷却析出黄色结晶固体,过滤干燥得黄色固体4-甲基-5-乙酰硫基-2-氟-N-乙酰苯胺(Ⅳ)3.94 g,收率71.9%,熔点94.2~96.1℃。1H NMR(600 MHz,CDCl3)δ:9.14(s,1H),7.53(d,J=5.0 Hz,1H),7.04(d,J=8.1 Hz,1H),2.39(s,3H),2.38(s,3H),2.17(s,3H)。ESI-MS(m/z):[M+H]+测试值242.06。
3.4 中间体4-甲基-2-氟-5-巯基苯胺(Ⅴ)的合成
向250mL三口瓶中加入4-甲基-5-乙酰硫基-2-氟-N-乙酰苯胺(Ⅳ)3.94 g(16.34 mmol)、氢氧化钾2.93 g(52.21 mmol)、水26.50 g,搅拌升温至90℃并保温5 h。TLC监测反应结束,反应液滴入50 mL冰水中,用2 mol/L的盐酸调节pH至2。萃取,有机相用无水硫酸镁干燥,减压旋蒸,干燥得灰白色固体4-甲基-2-氟-5-巯基苯胺(Ⅴ)2.31 g,收率90.0%,熔点93.4~94.5℃,1H NMR(600 MHz,CDCl3)δ:6.76~6.69(m,2H),5.69(s,1H),4.38(d,J=6.4 Hz,1H),4.27(d,J=6.6 Hz,1H),2.37(s,3H)。ESI-MS(m/z):[M+H]+测试值158.04。
3.5 中间体4-甲基-2-氟-5-(2,2,2-三氟乙硫基)苯胺(Ⅵ)的合成
向50 mL三口瓶中加入碳酸钾3.53 g(25.54 mmol)、甲醛次硫酸钠二水合物1.30 g(9.41 mmol)、4-甲基-2-氟-5-巯基苯胺(Ⅴ)2.01 g(12.80 mmol)和25 mL N,N-二甲基甲酰胺。向反应体系中滴入2,2,2-三氟碘乙烷3.08 g(14.67 mmol),滴加完毕后室温下搅拌2 h。TLC监测反应结束,反应液滴入50 mL水中,萃取,有机相用无水硫酸镁干燥,减压旋蒸,得红色油状的粗产物。粗产物经柱层析纯化得到黄色油状物,即中间体4-甲基-2-氟-5-(2,2,2-三氟乙硫基)苯胺(Ⅵ)2.11 g,产率68.9%。1H NMR(600 MHz,CDCl3)δ:6.83(d,J=8.0 Hz,1H),6.67(d,J=5.0 Hz,1H),4.26(s,2H),3.52(q,J=9.0 Hz,2H),2.36(s,3H)。ESI-MS(m/z):[M+H]+测试值240.04。
3.6 中间体SD-01的合成
向50 mL三口瓶中加入1,1,1-三氟-2-异硫氰基乙烷2.00 g(14.17 mmol)、碳酸钾2.16 g(15.63 mmol)、溴乙酸甲酯2.16 g(14.12 mmol)和5 mL甲苯,搅拌升温至50℃。向反应体系缓慢滴加4-甲基-2-氟-5-(2,2,2-三氟乙硫基)苯胺(Ⅵ)1.2 g(5.02 mmol),30 min滴加完毕并搅拌2 h。TLC监测反应结束,反应液滴入100 mL水中,萃取,有机相用无水硫酸镁干燥,经柱层析纯化后得到橘黄色油状物1.3 g,即中间体SD-01,产率61.7%。1H NMR(600 MHz,CDCl3)δ:7.12(d,J=5.0 Hz,1H),6.92(d,J=8.1 Hz,1H),4.52(q,J=9.1 Hz,2H),3.93(s,2H),3.52(q,J=9.1 Hz,2H),2.35(s,3H)。ESI-MS(m/z):[M+H]+测试值421.02。
3.7 目标化合物sulfiflumin的合成
向25 mL单口瓶中加入0.75 mL二氯甲烷和10.3 mg(0.029 mmol)乙酰丙酮铁。依次加入2,4-二氯-6-((E)-(((2R)-1-羟基-3,3-二甲基丁-2-基)亚氨基)甲基)苯酚17 mg(0.059 mmol)、苯甲酸钠8.4 mg(0.058 mmol)、(2Z)-2-((2-氟-4-甲基-5-((2,2,2-三氟乙基)硫基)苯基)亚氨基)-3-(2,2,2-三氟乙基)-1,3-噻唑烷-4-酮(SD-01)246 mg(0.585 mmol)、二氯甲烷0.7 mL。20~22°C下,向此混合体系中缓慢滴加34%过氧化氢水溶液165.9 mg(1.66 mmol)。搅拌1 h后,HPLC分析显示原料完全转化,萃取,有机相用无水硫酸镁干燥,经柱层析纯化后得到淡黄色固体目标物sulfiflumin 238.7 mg,产率93.6%,熔点106.1~107.5℃,ee值为98.9%。1H NMR(600 MHz,CDCl3)δ:7.46(d,J=5.0 Hz,1H),7.21(d,J=8.1 Hz,1H),4.52(q,J=9.1 Hz,2H),3.93(s,2H),3.64(q,J=9.0 Hz,2H),2.45(s,3H)。ESI-MS(m/z):[M+H]+测试值437.02。
4. 生物活性测试
采用叶片喷雾法测试供试化合物对朱砂叶螨的杀成螨活性。首先,将准确称量的供试化合物(SD-01和sulfiflumin)溶于少量丙酮与甲醇的混合溶剂中,然后用含0.2%(体积分数)吐温80的水溶液稀释,配制成一系列梯度浓度的药液。试验以市售杀螨剂乙唑螨腈(cyetpyrafen)作为对照药剂,以不含供试化合物的溶剂溶液作为空白对照。
选取温室培养的健康菜豆幼苗,待其长出2片真叶后,于每片叶上接种健康的朱砂叶螨雌成螨,并记录初始螨数。随后,使用手持喷雾器将各浓度药液均匀喷洒于整株菜豆苗的叶片上。每处理设置3次重复。处理后的植株置于标准条件的人工气候室中培养,48 h后检查并记录各处理的存活螨数。死亡率根据式(1)计算,并采用Abbott公式进行校正。
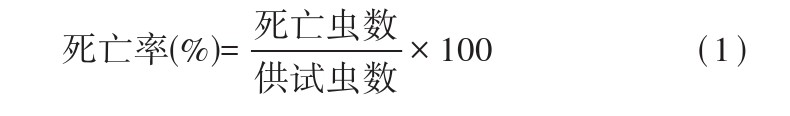
5. 分子对接
为预测配体与受体间的相互作用,本研究开展了分子对接(半柔性对接)。以重组人乙酰胆碱酯酶(PDB ID:4EY7)的晶体结构作为受体蛋白,将经过能量优化的sulfiflumin分子作为配体。
采用AutoDock 1.5.6软件计算sulfiflumin与靶标蛋白的结合模式和相互作用能。对接完成后,选取最优结果,并使用Discovery Studio 4.5 Client软件进行可视化,以分析二者之间的详细相互作用。
6. Gaussian计算
采用Gaussian 16软件包,通过密度泛函理论(DFT)方法,选用B3LYP泛函和6-311G(d)基组,对SD-01与sulfiflumin的不同构象进行几何优化,以确定其能量极小值点。在此基础上,计算并分析了各稳定构象之间的能级差(ΔE)。
结果与讨论
1. 生物活性测试
为评估sulfiflumin及SD-01对朱砂叶螨成螨的杀螨活性,本研究进行了室内生物测定试验,结果汇总于表1。
表1 SD-01、sulfiflumin的杀螨活性
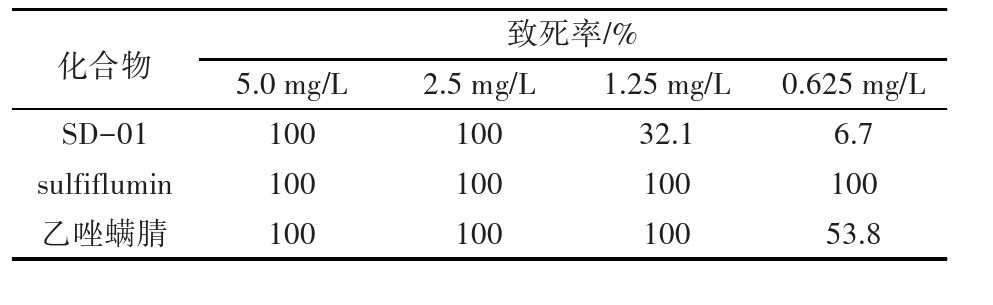
根据表1所示数据,在5.0、2.5 mg/L的质量浓度下,sulfiflumin与SD-01均表现出100%的朱砂叶螨成螨致死率。当质量浓度降低至1.25、0.625 mg/L时,sulfiflumin的致死率仍维持在100%,而SD-01的致死率则分别为32.1%和6.7%。结果表明,在所测试浓度范围内,sulfiflumin对朱砂叶螨成螨的杀螨活性显著优于SD-01以及作为对照的乙唑螨腈。
2. 相互作用模式研究
2.1 分子对接
为初步阐明sulfiflumin的杀螨作用机制,以重组人乙酰胆碱酯酶为靶标蛋白,利用AutoDock 1.5.6软件进行了分子对接试验。对接结果(如图3所示)表明,sulfiflumin分子能够有效嵌入到受体蛋白的活性口袋中。其三氟乙基及芳香环结构与周围的氨基酸残基存在显著的疏水相互作用。此外,sulfiflumin分子中的S=O基团与受体蛋白的ARG-296残基形成一条长度为2.1Å的氢键,而苯环连接的N原子则与THR-238残基形成另一条长度为2.2Å的氢键。根据相关文献报道,氢键长度小于3Å通常被认为具有良好的强度和稳定性。
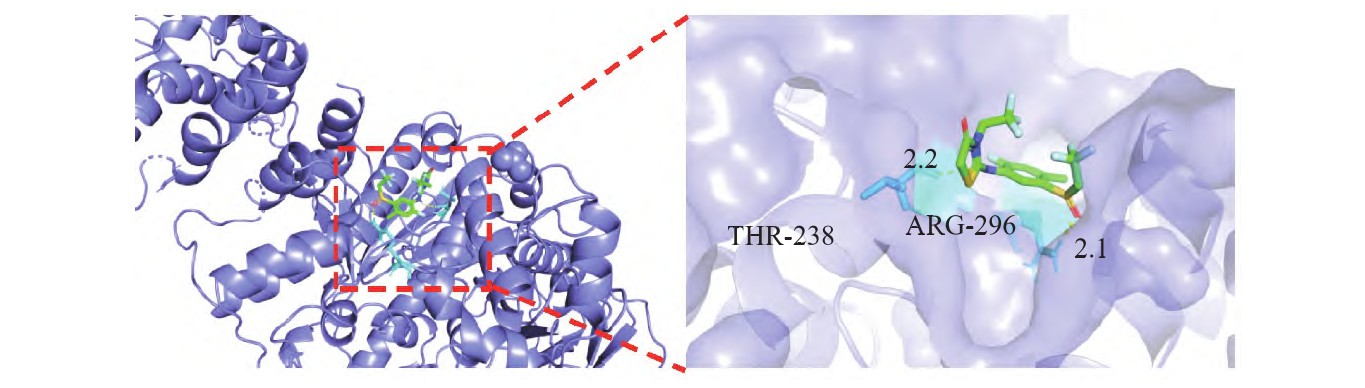
图3 Sulfiflumin与受体对接3D模式示意图
2.2 Gaussian计算
本实验利用Gaussian 16程序,采用密度泛函理论方法,选用B3LYP泛函和6-311G(d)基组,分别对SD-01和sulfiflumin进行了单点能级计算。结果显示(见图4),SD-01分子的最高占据分子轨道(HOMO)与最低未占据分子轨道(LUMO)之间的能级差(ΔE)为510.34 kJ/mol,而sulfiflumin的相应能级差为505.44 kJ/mol,二者之间相差4.90 kJ/mol。
HOMO-LUMO能隙是衡量分子电子激发和反应活性的重要参数。通常,较小的能隙预示着分子更容易发生电子跃迁,从而可能表现出更高的生物活性。本实验的计算结果表明,sulfiflumin具有相对较小的HOMO-LUMO能隙。这种能级差的差异可能与2种化合物的结构特征有关:sulfiflumin分子中S=O键的电子效应可能影响了其分子轨道能量的分布,导致HOMO-LUMO能隙变窄,电子云更容易极化。这可能为sulfiflumin表现出更优异的杀螨活性提供了一定的理论解释。
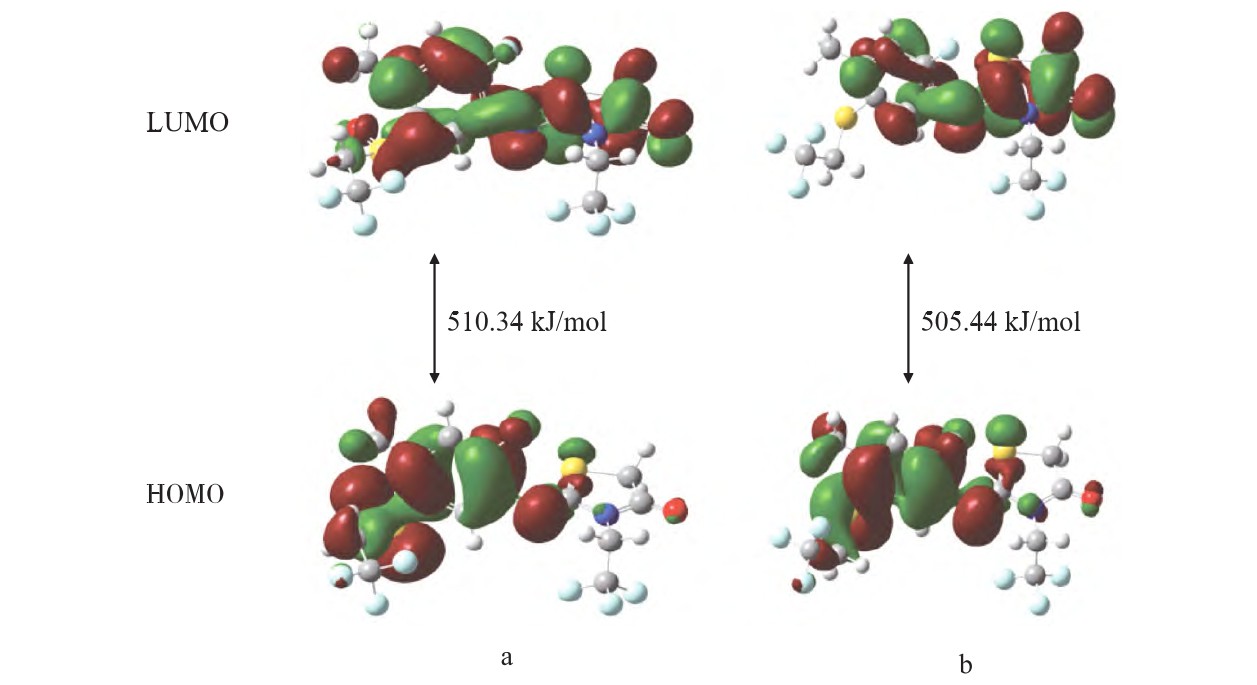
图4 SD-01(a)与sulfiflumin(b)的能级差
结论
本实验以2-氟-4-甲基苯胺为起始原料,通过6步反应成功合成了三氟乙基硫醚类化合物SD-01,并进一步经手性氧化得到具有R-构型亚砜结构的sulfiflumin,合成路线具有反应条件温和、原料易得的优点。
生物活性测试结果表明,sulfiflumin对朱砂叶螨的杀螨活性显著优于其前体化合物SD-01。在1.25、0.625 mg/L质量浓度下,sulfiflumin保持100%致死率,而SD-01的致死率仅为32.1%和6.7%,表明亚砜官能团的引入大幅提升了化合物的杀螨效力。Sulfiflumin在农业害螨综合防治领域展现出重要的应用潜力。
分子模拟研究从理论层面揭示了活性差异的可能机制:分子对接显示sulfiflumin能够与乙酰胆碱酯酶形成稳定的氢键相互作用;Gaussian量子化学计算表明:相比于SD-01(ΔE=510.34 kJ/mol), sulfiflumin具有更小的HOMO-LUMO能隙(ΔE=505.44 kJ/mol),分子电子云更易极化,可能有利于与生物靶标的结合。
本实验证实了硫醚向亚砜的氧化转化是提高三氟乙基硫醚类化合物杀螨活性的有效策略,为该类新型杀螨剂的分子设计与结构优化提供了重要的理论依据和实验基础。这一发现对于开发具有新颖作用机制的杀螨剂、应对害螨抗性问题具有重要的指导意义。
